Assimetrik induksiya
Stereokimyoda assimetrik induksiya (shuningdek, enantioinduktsiya) substratda, reagentda, katalizatorda yoki muhitda mavjud bo'lgan xiral xususiyatning ta'siri natijasida bir enantiomer yoki diastereoizomerning ikkinchisiga nisbatan kimyoviy reaksiyadagi imtiyozli shakllanishini tavsiflaydi.[1] Asimmetrik indüksiyon, assimetrik sintezda asosiy element hisoblanadi.
Asimmetrik induksiya Hermann Emil Fischer tomonidan uglevodlar ustidagi ishlariga asoslanib kiritilgan.[2] Induksiyaning bir necha turlari mavjud.
Ichki assimetrik induktsiya reaktiv markazga kovalent bog ' orqali bog'langan chiral markazdan foydalanadi va reaksiya davomida shunday bo'lib qoladi. Boshlang'ich material ko'pincha chiral hovuz sintezidan olinadi. O'tkazilayotgan assimetrik induktsiyada xiral ma'lumot alohida bosqichda kiritiladi va alohida kimyoviy reaksiyada yana olib tashlanadi. Maxsus sintonlar chiral yordamchilar deb ataladi. Tashqi assimetrik indüksiyonda chiral ma'lumot o'tish holatida chiral ligand katalizatori orqali kiritiladi. Asimmetrik sintezning bu usuli iqtisodiy jihatdan eng maqbuldir.
Karbonil 1,2 assimetrik induksiya
[tahrir | manbasini tahrirlash]Nukleofil qo'shimchalar paytida karbonil uglerodlarda xiral induksiyani tasvirlash uchun bir nechta modellar mavjud. Ushbu modellar sterik va elektron mulohazalar kombinatsiyasiga asoslanadi va ko'pincha bir-biriga zid keladi. Modellar Kram (1952), Kornfort (1959), Felkin (1969) va boshqalar tomonidan ishlab chiqilgan.
Kram qoidasi
[tahrir | manbasini tahrirlash]1952-yilda Donald J. Kram tomonidan ishlab chiqilgan assimetrik induksiyaning Kram qoidasi[3] ma'lum asiklik tizimlarda stereokimyoni bashorat qilish bilan bog'liq dastlabki tushunchadir. To'liq qoida:
Ba'zi katalitik bo'lmagan reaksiyalarda diastereomer ustunlik qiladi, bu esa C-C bog'ining aylanish konformatsiyasi qo'sh bog'lanish ikki eng kichik kattalikdagi ikkita guruh bilan yonma-yon joylashgan bo'lganda, eng kam to'siq bo'lgan tomondan kirish guruhining yaqinlashishi natijasida hosil bo'lishi mumkin..
Qoida shuni ko'rsatadiki, molekulada assimetrik markaz mavjudligi sterik to'siq asosida unga qo'shni bo'lgan assimetrik markazning shakllanishiga olib keladi.
O'zining 1952-yilgi nashrida Kram adabiyotda tavsiflangan ko'plab reaksiyalarni taqdim etdi, ular uchun reaksiya mahsulotlarining konformatsiyasi ushbu qoidaga asoslanib tushuntirilishi mumkin edi va u o'z ishini ko'rsatuvchi batafsil tajribani (sxema 1) tasvirlab berdi.
Tajribalar ikkita reaksiyani o'z ichiga oldi. Tajribada bitta 2-fenilpropionaldegid (1, rasemik, lekin (R)-enantiomer ko'rsatilgan) bromobenzolning Grignard reaktivi bilan diastereomerlar aralashmasi sifatida 1,2-difenil-1-propanol (2) ga reaksiyaga kirishdi, asosan treoizomer (Tushuntirish uchun Fisher proyeksiyasiga qarang).
Treoizomerning hosil bo'lishini afzal ko'rishni yuqorida aytib o'tilgan qoida bilan izohlash mumkin, chunki bu reaksiyada faol nukleofil karbonil guruhiga eng kam to'siq bo'lgan tomondan hujum qiladi (Qarang: Nyuman proyeksiyasi A). metil guruhi va vodorod atomi eng kichik sterik to'siqni yaratuvchi ikkita eng kichik o'rinbosar bo'lib, gauche orientatsiyasida va fenil antikonformatsiyadagi eng katta guruh sifatida.
Ikkinchi reaksiya 1,2-difenil-1-propanon 2 ning lityum alyuminiy gidrid bilan organik qaytarilishi bo'lib, yuqoridagi kabi bir xil reaksiya mahsulotiga olib keladi, ammo endi eritroizomer (2a) uchun afzallik beriladi. Endi gidrid anioni (H -) nukleofil eng kam to'siq bo'lgan tomondan hujum qiladi (vodorodning qog'oz tekisligidan kirib kelishini tasavvur qiling).
1952-yilgi asl nashrda Chugaev eliminatsiyasiga qo'llash orqali reaksiya mahsulotlarini strukturaviy belgilash uchun qo'shimcha dalillar olingan, bunda treoizomer --metil- stibenning sis izomeri va eritroizomer trans versiyasiga reaksiyaga kirishadi..
Felkin modeli
[tahrir | manbasini tahrirlash]Xyu Felkin nomidagi Felkin modeli (1968) ham karbonil guruhlarga nukleofil qo'shilish reaksiyalarining stereokimyosini bashorat qiladi. Felkinning ta'kidlashicha, Kram modeli katta kamchilikka duchor bo'lgan: karbonil o'rnini bosuvchi (aldegidlardagi vodorod atomi) va eng katta -karbonil o'rnini bosuvchi o'rtasidagi o'tish holatida tutilgan konformatsiya. U karbonil o'rnini bosuvchining sterik massasini metildan etilga, izopropildan izobutilga oshirish orqali stereoselektivlik ham ortib borishini ko'rsatdi, bu Kram qoidasida bashorat qilinmaydi:
Felkin qoidalari:
- O'tish holatlari reaktivga o'xshaydi.
- Qisman bog'lanishlarni o'z ichiga olgan burilish deformatsiyasi (Pitzer shtammi) (o'tish holatida), hatto bog'lanish darajasi juda past bo'lsa ham, to'liq hosil bo'lgan bog'lanishlar orasidagi deformatsiyaning muhim qismini ifodalaydi. TS dagi konformatsiya pogʻonali boʻlib, R oʻrnini bosuvchi ikkita qoʻshni guruhga nisbatan qiyshiqligi bilan tutilib turmaydi, ulardan biri TS Adagi eng kichiki.
- Taqqoslash uchun TS B - Cram o'tish holati.
- Asosiy sterik o'zaro ta'sirlar karbonil kislorod atomini emas, balki R va nukleofil atrofidagilarni o'z ichiga oladi.
- Nukleofilning hujumi karbonilga perpendikulyar emas, balki vodorodni ushlab turgan Dunitz burchagi (107 daraja) bo'yicha sodir bo'ladi.
- Polar effekt yoki elektron effekt nukleofil va elektronni tortib oluvchi guruh o'rtasidagi maksimal ajralish bilan o'tish holatini barqarorlashtiradi. Masalan, haloketonlar Kram qoidasiga bo'ysunmaydi va yuqoridagi misolda elektronni tortib oluvchi fenil guruhini siklogeksil guruhi bilan almashtirish stereoselektivlikni sezilarli darajada pasaytiradi.
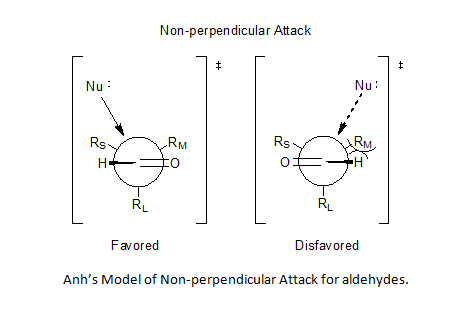
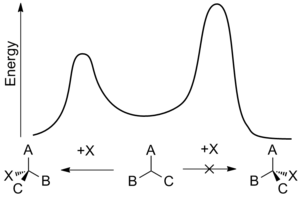
Felkin-Anh modeli
[tahrir | manbasini tahrirlash]Felkin-Anh modeli[4] Felkin modelining kengaytmasi boʻlib, u Nguyen Trọng Anh va Odil Eyzenshteyn tomonidan Felkin modelidagi ikkita asosiy zaiflikni tuzatish uchun taklif qilingan yaxshilanishlarni oʻz ichiga oladi. Ko'rib chiqilgan birinchi zaiflik Felkinning nukleofil qo'shilish o'tish holatlarida kuchli qutb effekti haqidagi bayonoti bo'ldi, bu SN2 reaksiyalari orqali stereokimyoning to'liq inversiyasiga olib keladi, bu hodisa nima uchun kuzatilganligi asoslantirilmaydi. Anhning yechimi assimetrik induksiyaning o'rnini bosuvchi va orbital effektlar bilan boshqarilishi natijasida antiperiplanar effektni taklif qilish edi.[5][6] Bu taʼsirda eng yaxshi nukleofil akseptor * orbital kiruvchi anionning barqarorlashuvini taʼminlovchi karbonilning ham , ham * orbitallariga parallel boʻladi.
Felkin modelidagi ikkinchi zaiflik karbonil R atrofida o'rinbosarlarni minimallashtirish taxmini edi, uni aldegidlarga qo'llash mumkin emas.
Burgi-Dunitz burchagi[7][8] gʻoyalarini birlashtirish Anhga kislorod-uglerod qoʻsh bogʻlanishiga nisbatan 95° dan 105° gacha boʻlgan har qanday joyda nukleofilning karbonil markaziga perpendikulyar boʻlmagan hujumini taxmin qilishga imkon berdi. kichikroq o'rinbosar va shu bilan aldegidlar uchun prognozlilik muammosini hal qiladi.[5][9][10]
Anti-Felkin selektivligi
[tahrir | manbasini tahrirlash]Kram va Felkin-Anh modellari ko'rib chiqilgan konformerlar va boshqa taxminlar bo'yicha farq qilsa-da, ularning ikkalasi ham bir xil asosiy hodisani tushuntirishga harakat qiladi: nukleofilning karbonil qismining eng sterik jihatdan qulay yuziga imtiyozli qo'shilishi. Biroq, Kram va Felkin-Anh modellarining asosiy qoidalarida bashorat qilinganidan farqli o'laroq, stereoselektivlikni aks ettiruvchi reaksiyalarning ko'plab misollari mavjud. Garchi ikkala modelda ham bu o'zgarishlarni tushuntirishga urinishlar mavjud bo'lsa-da, olingan mahsulotlar hali ham "anti-Felkin" mahsulotlar deb ataladi. O'zgartirilgan assimetrik induksiya selektivligining eng keng tarqalgan misollaridan biri Lyuis asosli komponent bilan almashtirilgan a-uglerodni talab qiladi (ya'ni O, N, S, P o'rinbosarlari). Bunday holatda, agar Al-iPr 2 yoki Zn2+ kabi Lyuis kislotasi kiritilsa, bidentat xelyatsiya effekti kuzatilishi mumkin. Bu karbonil va Lyuis asosi o'rnini bosuvchi konformatsiyani ushlab turadi va nukleofil keyin eng kichik erkin a-uglerod o'rnini bosuvchi tomondan hujum qiladi.[11] Agar xelatlovchi R guruhi eng katta deb aniqlansa, bu "anti-Felkin" mahsulotiga olib keladi.
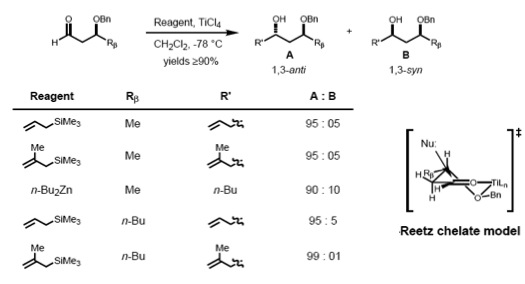
Ushbu stereoselektiv nazorat tan olingan va Cram modelini yaratuvchi birinchi maqolada muhokama qilingan, bu esa Kramni uning modeli xelatsiz shartlarni talab qilishini ta'kidlashiga sabab bo'lgan.[12] Reaksiyani xelatli nazorat qilish misolini bu erda, 1987-yilda chop etilgan maqoladan ko'rish mumkin, u birinchi bo'lib bunday "Kram-xelat" oraliq mahsulotini to'g'ridan-to'g'ri kuzatgan[13], bu modelni oqlaydi:
Bu yerda metil titan xlorid Cram-xelat hosil qiladi. Keyin metil guruhi titandan ajralib chiqadi va karbonilga hujum qiladi, bu esa anti-Felkin diastereomeriga olib keladi.
Xelatlanmaydigan elektronni tortib oluvchi o'rinbosar effekt ham Felkinga qarshi selektivlikka olib kelishi mumkin. Agar -ugleroddagi oʻrinbosar yetarlicha elektron tortib oladigan boʻlsa, nukleofil elektron tortib oluvchi guruhga nisbatan anti -ni qoʻshadi, hatto oʻrinbosar -uglerod bilan bogʻlangan 3 tadan eng kattasi boʻlmasa ham. Har bir model ushbu hodisa uchun biroz boshqacha tushuntirish beradi. Qutb effekti Kornfort modeli[14] va original Felkin modeli[15] tomonidan ilgari surilgan boʻlib, oʻtish strukturasining dipol momentini eng samarali tarzda bekor qilish uchun EWG oʻrnini bosuvchi va kiruvchi nukleofilni bir-biriga qarshi joylashtirgan.
Ushbu Nyuman proyeksiyasi Kornfort va Felkin o'tish holatini ko'rsatadi, bu EWG ni RS va RL ga nisbatan sterik massasidan qat'i nazar, kiruvchi nukleofilga qarshi joylashtiradi.
Yaxshilangan Felkin-Anh modeli, yuqorida muhokama qilinganidek, afzal o'tish holatini barqarorlashtirishda molekulyar orbital o'zaro ta'sirlarni hisobga olgan holda qutb effektini yanada murakkabroq baholashni amalga oshiradi. Ushbu ta'sirning potentsial anti-Felkin selektivligini ko'rsatadigan odatiy reaksiya, uning taklif qilingan o'tish tuzilishi bilan birga, quyida tasvirlangan:
Karbonil 1,3 assimetrik induksiya
[tahrir | manbasini tahrirlash]-uglerodidagi stereoelektronning muhit ham assimetrik induksiyani yo'naltirishi mumkinligi kuzatildi. Yillar davomida bunday reaksiyalarning stereoselektivligini aniqlash uchun bir qator bashoratli modellar ishlab chiqilgan.
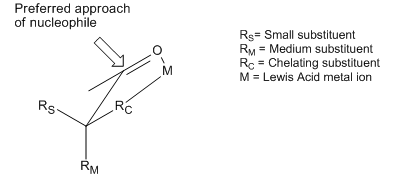
Xelatsiya modeli
[tahrir | manbasini tahrirlash]Reetzning fikriga ko'ra, 1,2-induksiya uchun Kram-xelat modeli -alkoksi aldegid va metallning xelatli kompleksini bashorat qilish uchun kengaytirilishi mumkin. Nukleofil kamroq sterik to'siq bo'lgan tomondan hujum qiladi va o'rnini bosuvchi R ga qarshi bo'lib, asosiy mahsulot sifatida antiadduktga olib keladi.[16]
Bunday xelatlarni hosil qilish uchun metall markazida kamida ikkita erkin koordinatsiya joyi bo'lishi kerak va himoya ligandlari Lyuis kislotasi bilan bidentat kompleksini hosil qilishi kerak.
Xelyatsiyasiz model
[tahrir | manbasini tahrirlash]Kram-Reetz modeli
[tahrir | manbasini tahrirlash]Kram va Rets, agar reaksiya asiklik o'tish holatida davom etsa, 1,3-stereo nazorat qilish mumkinligini ko'rsatdi. -alkoksi aldegidning alliltrimetilsilan bilan reaksiyasi anti-1,3-diol uchun yaxshi selektivlikni ko'rsatdi, bu Kram qutb modeli bilan izohlandi. Polar benziloksi guruhi dipol o'zaro ta'sirini kamaytirish uchun karbonilga qarshi yo'naltirilgan va nukleofil qolgan ikkita o'rinbosarning kattaligiga (RM) qarshi hujum qiladi.[17][18]
Evans modeli
[tahrir | manbasini tahrirlash]Yaqinda Evans xelatsiz 1,3-induksiyalar uchun boshqa modelni taqdim etdi. Tavsiya etilgan o'tish holatida, Felkin-Anh modelida ko'rsatilganidek, -stereosentr kiruvchi nukleofilga qarshi yo'naltirilgan. -stereotsentrdagi qutbli X guruhi dipol o'zaro ta'sirini kamaytirish uchun karbonilga qarshi joylashtiriladi va sterik to'siqni minimallashtirish uchun R aldegid guruhiga qarshi joylashtiriladi. Shunday qilib, 1,3- anti -diol asosiy mahsulot sifatida taxmin qilinadi.[19]
Karbonil 1,2 va 1,3 assimetrik induksiya
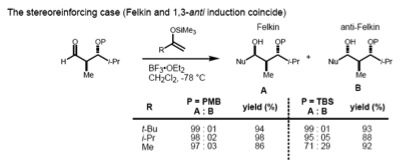
[tahrir | manbasini tahrirlash]Agar substrat ham - va -stereosentrga ega bo'lsa, Felkin-Anh qoidasi (1,2-induksiya) va Evans modeli (1,3-induksiya) bir vaqtning o'zida ko'rib chiqilishi kerak. Agar ushbu ikkita stereomarkazda anti-munosabat mavjud bo'lsa, ikkala model ham bir xil diastereomerni bashorat qiladi (stereomerkamlovchi holat).
Biroq, sin-substrat holatida, Felkin-Anh va Evans modeli turli xil mahsulotlarni bashorat qiladi (stereoreforcing bo'lmaan holat). Ma'lum bo'lishicha, kiruvchi nukleofilning o'lchami stereokimyoga nisbatan qo'llaniladigan nazorat turini belgilaydi. Katta nukleofil bo'lsa, -stereotsentrning kiruvchi nukleofil bilan o'zaro ta'siri dominant bo'ladi; shuning uchun Felkin mahsuloti asosiy hisoblanadi. Kichikroq nukleofillar esa assimetriyani aniqlaydigan 1,3 nazoratiga olib keladi.[20]
Asiklik alkenlar assimetrik induksiya
[tahrir | manbasini tahrirlash]Xiral asiklik alkenlar, shuningdek, epoksidlanish va enolat alkillanish kabi reaksiyalarda diasteroselektivlikni ko'rsatadi. Alken atrofidagi o'rinbosarlar elektrofilning molekulaning u yoki bu yuzidan yaqinlashishiga yordam berishi mumkin. Bu Kendall Xoukning nazariy ishlariga asoslangan Houk modelining asosi bo'lib, u selektivlik trans qo'sh bog'lanishlarga qaraganda cis uchun kuchliroq ekanligini taxmin qiladi.[21]
Ko'rsatilgan misolda sis alken RS va metil guruhi o'rtasidagi sterik to'qnashuvni minimallashtirish uchun ko'rsatilgan konformatsiyani qabul qiladi. Elektrofilning yondashuvi asosan ko'rsatilgan diastereoizomerni ishlab chiqaradigan katta guruh (RL) emas, balki o'rta guruhning (RM) bir tomonida sodir bo'ladi. Transalken uchun RS va H guruhi o'rtasidagi sterik to'siq sis holatidagidek katta bo'lmagani uchun selektivlik ancha past bo'ladi.
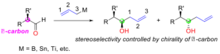
Substrat nazorati: asiklik tizimlarda molekulyar asos bilan assimetrik induksiya
[tahrir | manbasini tahrirlash]Asiklik substratning molekulyar doirasi tomonidan assimetrik induktsiya molekulaning assimetrik sterik va elektron xususiyatlari ushbu molekulada keyingi kimyoviy reaksiyalarning xiralligini aniqlashi mumkin degan fikrdir. Bu printsip bitta stereosentr mavjud bo'lgan va qo'shimcha stereosentrlar talab qilinadigan kimyoviy sintezlarni loyihalash uchun ishlatiladi.
Ikki funktsional guruh yoki turning qanday reaksiyaga kirishishini ko'rib chiqayotganda, ishtirok etgan kimyoviy ob'ektlarning aniq 3D konfiguratsiyasi ularning bir-biriga qanday yaqinlashishini aniqlaydi. Ushbu turlarning bir-biriga qanday yaqinlashishiga oid har qanday cheklovlar reaksiya mahsulotining konfiguratsiyasini aniqlaydi. Asimmetrik induksiya holatida biz bitta assimetrik markazning molekulaga ta'sirini boshqa funktsional guruhlarning ushbu molekuladagi reaktivligini ko'rib chiqamiz. Bu ikki ob'ekt bir-biriga qanchalik yaqin bo'lsa, ta'sir shunchalik katta bo'lishi kutiladi. Ushbu omillarni baholashda yanada yaxlit yondashuv hisoblash modellashtirishdir[22], ammo oddiy sifat omillari ham ba'zi sintetik qadamlar uchun kuzatilgan ustun tendentsiyalarni tushuntirish uchun ishlatilishi mumkin. Ushbu sifatli yondashuvning qulayligi va aniqligi uning sintez va substrat dizaynida ko'proq qo'llanilishini anglatadi. Tegishli molekulyar tuzilmalarga alfa chiral aldegidlar va chiral yordamchilardan foydalanish misol bo'ladi.
Alfa-xiral aldegidlarda assimetrik induksiya
[tahrir | manbasini tahrirlash]Aldegidlarda mumkin bo'lgan reaktivlikka nukleofil hujum va allilmetallarning qo'shilishi kiradi. Alfa-xiral aldegidlarda nukleofil hujumning stereoselektivligi Felkin-Anh yoki qutbli Felkin Anh modellari va axiral allilmetallarning qo'shilishi Kram qoidasi bilan tavsiflanishi mumkin.
Felkin-Anh va qutbli Felkin-Anh modeli
[tahrir | manbasini tahrirlash]Xiral aldegidlarga nukleofil qo'shilishlardagi selektivlik ko'pincha Felkin-Anh modeli bilan izohlanadi[23] (rasmga qarang). Nukleofil Burgi-Dunitz burchagida karbonil guruhining uglerodiga yaqinlashadi.[24] Ushbu traektoriyada qo'shni, katta, funktsional guruhning sterik katta qismi tufayli pastki yuzdan hujum nomaqbuldir.
Polar Felkin-Anh modeli X elektronegativ guruh bo'lgan ssenariyda qo'llaniladi. Polar Felkin-Anh modeli kuzatilgan stereokimyo C-X antibog'i * orbital va hosil qiluvchi bog' o'rtasidagi anti-periplanar o'zaro ta'sir natijasida kelib chiqadigan giperkonjugativ stabilizatsiya tufayli yuzaga keladi, deb taxmin qiladi.
Aldegidlarga organometal qo'shilishi uchun Felkin-Anh selektivligini yaxshilashga tegishli Grignard yoki organolitiy nukleofillari o'rniga organo-alyuminiy nukleofillaridan foydalanish orqali erishish mumkin. Klod Spino va uning hamkasblari[25] vinilgrignarddan bir qator xiral aldegidlar bilan vinilalan reagentlariga o'tishda sezilarli stereoselektivlikni ko'rsatdilar.
Kram qoidasi
[tahrir | manbasini tahrirlash]Aldegidlarga axiral allilmetallarning qo'shilishi xiral spirtini hosil qiladi, bu reaksiyaning stereokimyoviy natijasi aldegid substratidagi -uglerodning xiralligi bilan belgilanadi ("Substrat nazorati: axiral allilmetallarning -xiral aldegidlarga qo'shilishi" rasm). Qo'llaniladigan allilmetal reagentlar orasida bor, qalay va titan mavjud.
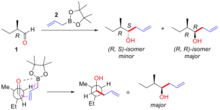
Kram qoidasi 3-rasmda tasvirlangan o'tish holatini hisobga olgan holda stereoselektivlikni tushuntiradi. O'tish holatida kislorodli juftlik bor markazi bilan o'zaro ta'sir o'tkazishi mumkin, allil guruhi esa karbonil guruhining uglerod uchiga qo'shila oladi. Ushbu o'tish holatining sterik talabi -uglerod konfiguratsiyasi eng katta guruhni tiqilib qolgan karbonil guruhidan uzoqda ushlab turadigan (trans-to) va allilmetal guruhi a-uglerod markazidagi eng kichik guruhdan o'tib, minimallashtiriladi. Quyidagi misolda ("Axiral allil-borning a-chiral aldegidga substrat bilan boshqariladigan qo'shilishi misoli" rasm), (R)-2-metilbutanal (1) allilboron reaktivi (2) bilan ikkita diastereomer bilan reaksiyaga kirishadi. (R, R)-izomer asosiy mahsulot hisoblanadi. Ushbu reaksiyaning Cram modeli karbonil guruhining etil guruhiga (katta guruh) o'tishi va allil borning vodorod (kichik guruh) yonidan o'tishi bilan ko'rsatilgan. Struktura Nyuman proyeksiyasida ko'rsatilgan. Bunday holda nukleofil qo'shilish reaksiyasi vodorod (kichik guruh) joylashgan yuzada sodir bo'lib, asosiy mahsulot sifatida (R, R)-izomerni hosil qiladi.
Chiral yordamchilar
[tahrir | manbasini tahrirlash]Asimmetrik stereoinduksiyaga chiral yordamchi vositalar yordamida erishish mumkin. Chiral yordamchi moddalar substratga teskari tarzda biriktirilishi mumkin, bu esa parchalanishdan oldin diastereoselektiv reaksiyani keltirib chiqaradi va umuman olganda enantioselektiv jarayonni keltirib chiqaradi. Chiral yordamchilarga misollar: Evansning chiral oksazolidinon yordamchilari (assimetrik aldol reaksiyalari uchun)[26] psevdoefedrin amidlari va tert-butansulfinamid iminlari.
Substrat nazorati: siklik tizimlarda molekulyar asos bilan assimetrik induksiya
[tahrir | manbasini tahrirlash]Siklik molekulalar ko'pincha chiziqli hamkasblariga qaraganda ancha qattiq konformatsiyalarda mavjud. Eritromitsin kabi juda katta makrotsikllar ham ko'p erkinlik darajasiga ega bo'lishiga qaramay, aniq geometriyalarda mavjud. Ushbu xususiyatlar tufayli ko'pincha chiziqli emas, balki makrosiklik substratlar bilan assimetrik induksiyaga erishish osonroq. V. Klark Still[27] va uning hamkasblari tomonidan amalga oshirilgan dastlabki tajribalar shuni ko'rsatdiki, o'rta va katta halqali organik molekulalar kinetik enolat alkilatsiyasi , dimetilkuprat qo'shilishi va katalitik gidrogenatsiya kabi reaksiyalarda substrat sifatida stereo induktsiyaning ajoyib darajasini ta'minlay oladi. Reaksiyaning diastereomerik natijasini o'zgartirish uchun hatto bitta metil guruhi ko'pincha etarli. Ushbu tadqiqotlar, jumladan, katta halqalar har qanday stereokimyoviy nazoratni ta'minlash uchun juda yumshoq ekanligi haqidagi keng tarqalgan ilmiy e'tiqodni rad etishga yordam berdi.
Bir qator umumiy sintezlar kerakli reaksiya mahsulotlariga erishish uchun makrosiklik stereokontroldan foydalangan. (-)-kladiella-6,11-dien-3-ol sintezida,[28] shtammli trialmashtirilgan olefin N -metilmorfolin N -oksid (NMO) va osmiy tetroksid bilan diasetereoselektiv dihidroksillangan. olefin. (±)-periplanon B ga yo'lda,[29] kimyogarlar boshqa ikkita alken borligida tert-butil gidroperoksid yordamida enon oraliq mahsulotining yuz selektiv epoksidlanishiga erishdilar. Seskiterpen evkannabinolidiga[30] 10 a'zoli halqali enon oraliq mahsulotining natriy borgidridining qisqarishi molekulyar modellashtirish hisob-kitoblarida bashorat qilinganidek, eng past energiya makrotsikl konformatsiyasini hisobga olgan. Substrat bilan boshqariladigan sintetik sxemalar juda ko'p afzalliklarga ega, chunki ular selektiv transformatsiyalarga erishish uchun murakkab assimetrik reagentlardan foydalanishni talab qilmaydi.
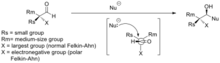
Reagent nazorati: axiral aldegidlarga chiral allilmetallarni qo'shish
[tahrir | manbasini tahrirlash]Organik sintezda reagentni boshqarish ko'pdan bitta stereoizomerni tanlab hosil qilish yondashuvidir, stereoselektivlik ishlatiladigan reagentning tuzilishi va xiralligi bilan belgilanadi. Axiral aldegidlarga nukleofil qo'shilish reaksiyasi uchun xiral allilmetallardan foydalanilganda, yangi hosil bo'lgan alkogolli uglerodning xiralligi allymetal reagentlarning xiralligi bilan aniqlanadi (1-rasm). Allimetallarning xiralligi odatda ishlatiladigan assimetrik ligandlardan kelib chiqadi. Allilmetal reagentlar tarkibidagi metallarga bor, qalay, titanium, kremniy va boshqalar kiradi.
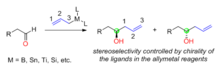
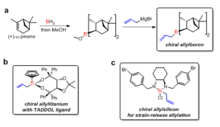
Xiral allilmetallarni aldegidlar bilan reaksiyaga tayyorlash uchun turli xil chiral ligandlar ishlab chiqilgan. HC Braun birinchi bo'lib aldegidlar bilan assimetrik allillanish reaksiyalari uchun chiral allilboron reagentlari haqida xabar berdi.[31] Chiral allilboron reagentlari tabiiy mahsulotdan (+)-a-pinendan ikki bosqichda sintez qilindi. Diter Seebach tomonidan ishlab chiqilgan TADDOL ligandlari aldegidlar bilan assimetrik allyasiya uchun chiral alliltitan birikmalarini tayyorlash uchun ishlatilgan.[32] Jim Leyton xiral allysilikon birikmalarini ishlab chiqdi, ularda halqa shtammining chiqishi stereoselektiv allyasiya reaksiyasini osonlashtirdi, bir qator axiral aldegidlar uchun 95% dan 98% gacha enantiomerik ortiqcha erishish mumkin edi.[33]
Yana qarang
[tahrir | manbasini tahrirlash]- Makrosiklik stereokontrol
- Sieplak effekti
Manbalar
[tahrir | manbasini tahrirlash]- ↑ IUPAC Gold Book definition Link
- ↑ Asymmetric Synthesis of Natural Products, Ari Koskinen ISBN 0-471-93848-3
- ↑ Studies in Stereochemistry. X. The Rule of "Steric Control of Asymmetric Induction" in the Syntheses of Acyclic Systems Donald J. Cram, Fathy Ahmed Abd Elhafez J. Am. Chem. Soc.; 1952; 74(23); 5828–5835. Abstract
- ↑ It bears mentioning that in Vyetnamese, the surname is given first, and so this would be better called the Felkin–Nguyen Model.
- ↑ 5,0 5,1 Anh, N. T.; Eisenstein, O. Nouv. J. Chim. 1977, 1, 61.
- ↑ Anh, N. T.; Eisenstein, O.; Lefour, J-M.; Dau, M-E. J. Am. Chem. Soc. 1973, 95, 6146.
- ↑ Bürgi, H. B.; Dunitz, J. D.; Shefter, E. J. Am. Chem. Soc. 1973, 95, 5065.
- ↑ Bürgi, H. B.; Dunitz, J. D.; Lehn, J. M.; Wipff, G. Tetrahedron 1974, 30, 1563.
- ↑ Anh, N. T.; Eisenstein, O. Tetrahedron Lett. 1976, 155.
- ↑ Anh, N. T. Top. Curr. Chem. 1980, 88, 146.
- ↑ Mengel A., Reiser O.Chem. Rev., 1999, 99 (5), 1191–1224.
- ↑ Cram DJ, Elhafez FA. J. Am. Chem. Soc.; 1952; 74(23); 5828–5835.
- ↑ Reetz MT, Hullmann M, Seitz T. Angew. Chem. Int. Ed. Engl. 1987. 26, 477–480.
- ↑ Cornforth JW, Cornforth MRH, Mathew KK. J. Chem.Soc. 1959, 112–127.
- ↑ Cherest M, Felkin H, Prudent N. Tetrahedron Lett. 1968, 18, 2199–2204.
- ↑ Reetz, M.T.; Jung, A. J. Am. Chem. Soc., 1983, 105, 4833.
- ↑ Leitereg, T.J.; Cram, D.J. J. Am. Chem. Soc. 1968, 90, 4011.
- ↑ Reetz. M.T.; Kesseler, K.; Jung, A. Tetrahedron Lett. 1984, 25, 729.
- ↑ Evans, D.A.; Duffy, J.L.; Dart, M.J. Tetrahedron Lett. 1994, 35, 8537.
- ↑ Evans, D.A.; Dart, M.J.; Duffy, J.L.; Yang, M.G. J.Am. Chem. Soc. 1996, 118, 4322.
- ↑ Clayden. Organic Chemistry. Oxford University Press, 2001 — 895 bet. ISBN 978-0-19-850346-0.
- ↑ Houk, K. N. et al., Science, 1986, 231, 1108-1117.
- ↑ a) Anh, N. T. Top. Curr. Chem. 1980, 88, 145–162; (b) Anh, N. T.; Eisenstein, O. Nouv. J. Chim. 1977, 1, 61–70; (c) Anh, N. T.; Eisenstein, O. Tetrahedron Lett. 1976, 26, 155–158.
- ↑ Burgi, H. B.; Dunitz, J. D.; Lehn, J. M.; Wipff, G. Tetrahedron. 1974. 12, 1563–1572.
- ↑ Spino, C.; Granger, M. C.; Boisvert, L.; Beaulieu, C. Tetrahedron Lett. 2002, 43, 4183–4185.
- ↑ Evans, D. A.; Bartroli, J.; Shih, T. L., Am. Chem. Soc., 1981, 103, 2127-2129.
- ↑ Still, W. C.; Galynker, I. Tetrahedron 1981, 37, 3981-3996.
- ↑ Kim, Hyoungsu; Lee, Hyunjoo; Kim, Jayoung; Kim, Sanghee; Kim, Deukjoon (2006-12-01). „A General Strategy for Synthesis of Both (6Z)- and (6E)-Cladiellin Diterpenes: Total Syntheses of (−)-Cladiella-6,11-dien-3-ol, (+)-Polyanthellin A, (−)-Cladiell-11-ene-3,6,7-triol, and (−)-Deacetoxyalcyonin Acetate“. Journal of the American Chemical Society. 128-jild, № 49. 15851–15855-bet. doi:10.1021/ja065782w. ISSN 0002-7863. PMID 17147397.
- ↑ Still, W. Clark (1979-04-01). „(.+-.)-Periplanone-B. Total synthesis and structure of the sex excitant pheromone of the American cockroach“. Journal of the American Chemical Society. 101-jild, № 9. 2493–2495-bet. doi:10.1021/ja00503a048. ISSN 0002-7863.
- ↑ Still, W. Clark; Murata, Shizuaki; Revial, Gilbert; Yoshihara, Kazuo (1983-02-01). „Synthesis of the cytotoxic germacranolide eucannabinolide“. Journal of the American Chemical Society. 105-jild, № 3. 625–627-bet. doi:10.1021/ja00341a055. ISSN 0002-7863.
- ↑ Brown, H. C.; Jadhav, P. K. J. Am. Chem. Soc. 1983, 105, 2092.
- ↑ Duthaler, R. O.; Hafner, A. Chem. Rev. 1992, 92, 807.
- ↑ Kinnaird, J. W. A.; Ng, P. Y.; Kubota, K.; Wang, X.; Leighton, J. L. J. Am. Chem. Soc. 2002, 124, 7920.