Ion bog'lanish

Ionli bogʻlanish kimyoviy bogʻlanishning bir turi boʻlib, u qarama-qarshi zaryadlangan ionlar yoki elektromanfiyligi keskin farq qiluvchi ikki atom oʻrtasidagi elektrostatik tortishishni oʻz ichiga oladi[1] va ionli birikmalarda yuzaga keladigan asosiy oʻzaro taʼsirdir. Kovalent bog'lanish va metall bog'lanish bilan birga bog'lanishning asosiy turlaridan biridir. Ionlar elektrostatik zaryadga ega bo'lgan atomlar (yoki atomlar guruhlari). Elektron olgan atomlar manfiy zaryadlangan ionlarni (anionlar deb ataladi) hosil qiladi. Elektronlarni yo'qotadigan atomlar musbat zaryadlangan ionlarni (kationlar deb ataladi) hosil qiladi. Elektronlarning bunday uzatilishi kovalentlikdan farqli ravishda elektrovalentlik deb nomlanadi. Eng oddiy holatda, kation metall atomi, anion esa metall bo'lmagan atomdir, lekin bu ionlar yanada murakkab tabiatga ega bo'lishi mumkin, masalan, NH+ kabi molekulyar ionlar.NH</br> NH yoki SO2−</br> SO. Oddiyroq qilib aytganda, ion bog'lanish har ikkala atom uchun ham to'liq valentlik qobig'ini olish uchun elektronlarning metalldan metall bo'lmaganga o'tishi natijasida yuzaga keladi.
Bir atom yoki molekula to'liq elektronni boshqasiga o'tkazadigan toza ionli bog'lanish mavjud bo'lmasligini tan olish muhimdir: barcha ionli birikmalar ma'lum darajada kovalent bog'lanish yoki elektron almashishga ega. Shunday qilib, "ionli bog'lanish" atamasi ion xarakteri kovalent xarakterdan katta bo'lsa, ya'ni ikki atom o'rtasida katta elektron manfiylik farqi mavjud bo'lgan bog'lanish beriladi, bu esa bog'lanishning qutbli (ionli) bo'lishiga olib keladi. elektronlar teng taqsimlangan kovalent bog'lanish. Qisman ion va qisman kovalent xarakterga ega bo'lgan bog'lanishlar qutbli kovalent bog'lanishlar deyiladi.
Ion birikmalari erigan yoki eritma holatida elektr tokini o'tkazadi , odatda qattiq holatda emas. Ion birikmalari odatda yuqori erish nuqtasiga ega bo'lib, ular tarkibidagi ionlarning zaryadiga qarab. Zaryadlar qanchalik yuqori bo'lsa, birlashtiruvchi kuchlar shunchalik kuchli bo'ladi va erish nuqtasi shunchalik yuqori bo'ladi. Ular suvda ham eriydi ; birlashtiruvchi kuchlar qanchalik kuchli bo'lsa, eruvchanligi shunchalik past bo'ladi.
Umumiy koʻrinish[tahrir | manbasini tahrirlash]
Deyarli to'liq yoki deyarli bo'sh valent qobig'iga ega bo'lgan atomlar juda reaktiv bo'ladi. Kuchli elektronegativ bo'lgan atomlar (galogenlarda bo'lgani kabi) ko'pincha valentlik qobig'ida faqat bitta yoki ikkita bo'sh orbitalga ega va ko'pincha boshqa molekulalar bilan bog'lanadi yoki anionlarni hosil qilish uchun elektron oladi. Kuchsiz elektromanfiy atomlar (masalan, ishqoriy metallar) nisbatan kam valentlik elektronlariga ega boʻlib, ular kuchli elektronegativ boʻlgan atomlar bilan oson taqsimlanishi mumkin. Natijada, kuchsiz elektron manfiy atomlar elektron bulutini buzadi va kationlarni hosil qiladi.
Shakllanish[tahrir | manbasini tahrirlash]
Ionlanish energiyasi past bo'lgan element atomlari (odatda metall) barqaror elektron konfiguratsiyasiga erishish uchun elektronlarning bir qismini berganida, ionli bog'lanish oksidlanish -qaytarilish reaksiyasidan kelib chiqishi mumkin. Bunda kationlar hosil bo'ladi. Elektron yaqinligi yuqori bo'lgan boshqa elementning atomi (odatda metall bo'lmagan) barqaror elektron konfiguratsiyasiga erishish uchun bir yoki bir nechta elektronni qabul qiladi va elektronlarni qabul qilgandan so'ng atom anionga aylanadi. Odatda, barqaror elektron konfiguratsiyasi s-gruppa va p-gruppadagi elementlar uchun olijanob gazlardan biri va d-gruppa va f-gruppa elementlari uchun alohida barqaror elektron konfiguratsiyalardir. Anionlar va kationlar orasidagi elektrostatik tortishish kristallografik panjarali qattiq jismning hosil bo'lishiga olib keladi, unda ionlar o'zgaruvchan tarzda joylashadi. Bunday panjarada odatda diskret molekulyar birliklarni ajratib bo'lmaydi, shuning uchun hosil bo'lgan birikmalar molekulyar xarakterga ega emas. Biroq, ionlarning o'zi murakkab bo'lishi mumkin va atsetat anioni yoki ammoniy kationi kabi molekulyar ionlarni hosil qilishi mumkin.

Masalan, oddiy osh tuzi natriy xloriddir. Natriy (Na) va xlor (Cl) birlashganda, natriy atomlarining har biri elektronni yo'qotib, kationlarni (Na +) hosil qiladi va xlor atomlarining har biri anionlarni (Cl -) hosil qilish uchun elektron oladi. Keyin bu ionlar natriy xlorid (NaCl) hosil qilish uchun 1:1 nisbatda bir-biriga tortiladi.
- Na + Cl → Na + + Cl - → NaCl
Biroq, zaryadning neytralligini saqlash uchun anionlar va kationlar o'rtasidagi qat'iy nisbatlar kuzatiladi, shuning uchun ionli birikmalar, umuman olganda, molekulyar birikmalar bo'lmasa ham, stoxiometriya qoidalariga bo'ysunadi. Qotishmalarga o'tuvchi va aralash ion va metall bog'lanishga ega bo'lgan birikmalar uchun endi bunday bo'lmasligi mumkin. Ko'pgina sulfidlar, masalan, stoxiometrik bo'lmagan birikmalar hosil qiladi.
Ko'pgina ionli birikmalar tuzlar deb ataladi, chunki ular NaOH kabi Arrenius asosining neytrallanish reaksiyasi natijasida HCl kabi Arrenius kislotasi bilan hosil bo'lishi mumkin
NaOH + HCl → NaCl + H2O
Kation hosil qilish uchun elektronlarni olib tashlash endotermik bo'lib, tizimning umumiy energiyasini oshiradi. Mavjud aloqalarning uzilishi yoki anionlarni hosil qilish uchun bir nechta elektron qo'shilishi bilan bog'liq energiya o'zgarishlari ham bo'lishi mumkin. Biroq, anionning kationning valentlik elektronlarini qabul qilish harakati va ionlarning bir-biriga keyingi tortilishi (panjara) energiyani chiqaradi va shu bilan tizimning umumiy energiyasini pasaytiradi.
Reaksiya uchun umumiy energiya o'zgarishi qulay bo'lgan taqdirdagina ionli bog'lanish sodir bo'ladi. Umuman olganda, reaksiya ekzotermik, lekin, masalan, simob oksidi (HgO) hosil bo'lishi endotermikdir. Hosil bo'lgan ionlarning zaryadi ionli bog'lanish kuchining asosiy omili hisoblanadi, masalan, C + A tuzi Kulon qonuniga ko'ra C 2+ A 2− dan taxminan to'rt baravar kuchsiz elektrostatik kuchlar ta'sirida ushlab turiladi, bunda C va A mos ravishda generik kation va anionni ifodalaydi. Ushbu soddalashtirilgan argumentda ionlarning o'lchamlari va panjaraning o'ziga xos o'rami e'tiborga olinmaydi.
Tuzilmalar[tahrir | manbasini tahrirlash]
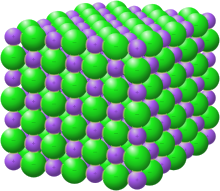
Qattiq holatda ionli birikmalar panjara tuzilmalarini hosil qiladi. Panjara shaklini aniqlashda ikkita asosiy omil - ionlarning nisbiy zaryadlari va ularning nisbiy o'lchamlari. Ba'zi tuzilmalar bir qator birikmalar tomonidan qabul qilinadi; Masalan, tosh tuzi natriy xloridning tuzilishi ko'plab gidroksidi galogenidlar va magniy oksidi kabi ikkilik oksidlar tomonidan ham qabul qilinadi. Pauling qoidalari ion kristallarining kristall tuzilmalarini bashorat qilish va ratsionalizatsiya qilish uchun ko'rsatmalar beradi.
Bog'lanishning mustahkamligi[tahrir | manbasini tahrirlash]
Qattiq kristalli ionli birikma uchun gazsimon ionlardan qattiq moddani hosil qilishdagi entalpiya o'zgarishi panjara energiyasi deb ataladi. Panjara energiyasining eksperimental qiymati Born-Haber sikli yordamida aniqlanishi mumkin. Bundan tashqari, Born-Landé tenglamasidan foydalanib, kationlar va anionlar o'rtasidagi o'zaro ta'sirlarni yig'ish orqali hisoblangan elektrostatik potentsial energiyaning yig'indisi va qisqa masofali itaruvchi potentsial energiya termini sifatida hisoblash (prognoz qilish) mumkin. Elektrostatik potentsial kristallning geometriyasini hisobga oladigan interion ajralish va doimiy (Madelung doimiysi) bilan ifodalanishi mumkin. Yadrodan qanchalik uzoq bo'lsa, qalqon shunchalik zaif bo'ladi. Born-Landé tenglamasi, masalan, natriy xloridning panjara energiyasiga mos ravishda mos keladi, bu erda hisoblangan (bashorat qilingan) qiymat -756 ga teng. kJ/mol, bu -787 ga teng Born-Haber siklidan foydalangan holda kJ/mol.[2] Suvli eritmada bog'lanish kuchini Bjerrum yoki Fuoss tenglamalari orqali ionlarning tabiatiga bog'liq bo'lmagan holda, qutblanish yoki kattalik kabi tavsiflash mumkin Tuz ko'priklarining mustahkamligi ko'pincha katyonik va anion joylarni o'z ichiga olgan molekulalar o'rtasidagi muvozanat, ko'pincha eritmada. Suvdagi muvozanat konstantalari har bir tuz ko'prigi uchun qo'shimchalarsiz energiya hissalarini ko'rsatadi. Murakkab molekulalarda ham vodorod aloqalarini aniqlashning yana bir usuli bu kristallografiya, ba'zan esa NMR-spektroskopiyadir.
Polarizatsiya quvvat effektlari[tahrir | manbasini tahrirlash]
Sof ionli birikmalarning kristall panjaralaridagi ionlar sharsimon ; ammo, agar musbat ion kichik va/yoki yuqori zaryadlangan bo'lsa, u manfiy ionning elektron bulutini buzadi, bu ta'sir Fajans qoidalarida umumlashtirilgan. Salbiy ionning bu qutblanishi ikki yadro o'rtasida qo'shimcha zaryad zichligining to'planishiga , ya'ni qisman kovalentlikka olib keladi. Kattaroq manfiy ionlar osonroq qutblanadi, lekin ta'sir odatda zaryadlari 3+ bo'lgan musbat ionlar (masalan, Al 3+) ishtirok etgandagina muhim bo'ladi. Biroq, 2+ ion (Be 2+) yoki hatto 1+ (Li +) ba'zi qutblanish kuchini ko'rsating, chunki ularning o'lchamlari juda kichik (masalan, LiI ionli, ammo kovalent bog'lanish mavjud). E'tibor bering, bu elektr maydonining qo'llanilishi tufayli panjaradagi ionlarning siljishiga ishora qiluvchi ion polarizatsiya effekti emas.
Kovalent bog'lanish bilan solishtirish[tahrir | manbasini tahrirlash]
Ion bog'lanishda atomlar qarama-qarshi zaryadlangan ionlarning tortilishi bilan bog'lanadi, kovalent bog'lanishda esa atomlar barqaror elektron konfiguratsiyasiga erishish uchun elektronlarni almashish orqali bog'lanadi. Kovalent bog'lanishda har bir atom atrofidagi molekulyar geometriya valentlik qobig'ining elektron juft repulsiyasi VSEPR qoidalari bilan belgilanadi, ionli materiallarda esa geometriya maksimal qadoqlash qoidalariga amal qiladi. Aytish mumkinki, kovalent bog'lanish ko'proq yo'naltirilgan, ya'ni optimal bog'lanish burchaklariga yopishmaslik uchun energiya jazosi katta, ion bog'lanish esa bunday jazoga ega emas. Bir-birini qaytarish uchun umumiy elektron juftlari yo'q, ionlar iloji boricha samarali tarzda to'planishi kerak. Bu ko'pincha ancha yuqori muvofiqlashtirish raqamlariga olib keladi. NaCl da har bir ion 6 ta bog'ga ega va barcha bog'lanish burchaklari 90 ° dir. CsCl da koordinatsion raqam 8 ga teng. Taqqoslash uchun uglerod odatda maksimal to'rtta aloqaga ega.
Sof ionli bog'lanish mavjud bo'lishi mumkin emas, chunki bog'lanishda ishtirok etuvchi ob'ektlarning yaqinligi ular o'rtasida ma'lum darajada elektron zichligini taqsimlash imkonini beradi. Shuning uchun barcha ionli bog'lanishlar qandaydir kovalent xususiyatga ega. Shunday qilib, ion xarakteri kovalent xarakterdan katta bo'lsa, bog'lanish ion hisoblanadi. Bog'lanishda ishtirok etuvchi ikki turdagi atomlar orasidagi elektronegativlikdagi farq qanchalik katta bo'lsa, u shunchalik ionli (qutbli) bo'ladi. Qisman ion va qisman kovalent xarakterga ega bo'lgan bog'lanishlar qutbli kovalent bog'lanishlar deyiladi. Masalan, Na-Cl va Mg-O o'zaro ta'siri bir necha foiz kovalentlikka ega, Si-O aloqalari odatda ~50% ion va ~50% kovalentdir. Pauling 1,7 (Pauling shkalasi bo'yicha) elektromanfiylik farqi 50% ion xarakteriga to'g'ri keladi, deb hisobladi, shuning uchun 1,7 dan katta farq asosan ionli bo'lgan bog'lanishga to'g'ri keladi.[3]
Kovalent bog'lanishlardagi ion xarakterini to'g'ridan-to'g'ri to'rt qutbli yadrolarga ega bo'lgan atomlar uchun o'lchash mumkin (2 H, 14 N, 81,79 Br, 35,37 Cl yoki 127 I). Ushbu yadrolar odatda NQR yadroviy to'rt kutupli rezonans va NMR yadro magnit aks sadolarini o'rganish ob'ektlari hisoblanadi. Yadro quadrupol momentlari Q va elektr maydon gradientlari (EFG) o'rtasidagi o'zaro ta'sir yadro to'rt kutupli ulanish konstantalari orqali tavsiflanadi.
- QCC =e2qzzQ/h
buerda eq zz termini EFG tenzorining bosh komponentiga mos keladi va e elementar zaryaddir. O'z navbatida, elektr maydon gradienti QCC qiymatlari NMR yoki NQR usullari bilan aniq aniqlanganda molekulalardagi bog'lanish rejimlarini tavsiflashga yo'l ochadi.
Umuman olganda, ionli bog'lanish qattiq (yoki suyuq) holatda sodir bo'lganda, ikkita alohida atom o'rtasidagi yagona "ionli bog'lanish" haqida gapirish mumkin emas, chunki panjarani bir-biriga bog'lab turuvchi qo'zg'alish kuchlari ko'proq kollektiv xarakterga ega. Bu kovalent bog'lanish holatida juda farq qiladi, bu erda biz ko'pincha ikkita alohida atom o'rtasida joylashgan aniq bog'lanish haqida gapirishimiz mumkin. Biroq, ionli bog'lanish ba'zi bir kovalentlik bilan birlashtirilgan bo'lsa ham, natijada mahalliylashtirilgan xarakterdagi diskret bog'lanishlar bo'lishi shart emas. Bunday hollarda, hosil bo'lgan bog'lanish ko'pincha butun kristallni qamrab olgan ulkan molekulyar orbitallardan tashkil topgan tarmoqli tuzilishi nuqtai nazaridan tavsifni talab qiladi. Shunday qilib, qattiq jismdagi bog'lanish ko'pincha mahalliylashtirilgan emas, balki kollektiv tabiatini saqlab qoladi. Elektromanfiylikdagi farq kamayganida, bog'lanish yarimo'tkazgich, yarim metall yoki oxir-oqibat metall bog'langan metall o'tkazgichga olib kelishi mumkin.
Yana qarang[tahrir | manbasini tahrirlash]
- Kulon qonuni[sayt ishlamaydi]
- Tuz ko'prigi (oqsil va supramolekulyar)[sayt ishlamaydi]
- Ion potentsiali
- Atom orbitallarining chiziqli birikmasi
- Gibridlanish
- Kimyoviy qutblanish
- Ioliomika
- Elektron konfiguratsiyasi
- Aufbau printsipi
- Kvant raqamlari
- Azimutal kvant soni
- Bosh kvant soni
- Magnit kvant soni
- Spin kvant soni
Manbalar[tahrir | manbasini tahrirlash]
- "Ionik aloqa"[sayt ishlamaydi] IYUPAC kimyoviy to'plami Termenologiya 2009.doi:10.1352/goldbook.IT0705058
- Shnayder Xans-Yorg (2012)"Supramolekulyar komplekslardagi ionli o'zaro ta'sirlar'' Tabiatdagi ionli o'zaro ta'sirlar va sintetik makromolekulalar.35-47-betlar doi.10.1002/9781118165850.ch2
- David Artur Jonson Metallar va kimyoviy o'zgarishlar Ochiq universiteti,Qirollik kimyo jamiyati 2002, ISBN 0-854040-665-8
Havolalar[tahrir | manbasini tahrirlash]
- Ion bog'lanish bo'yicha qo'llanma
- Ion bog'lanish haqida video
- ion bog'lanish xususiyatlari (Wayback Machine saytida 2013-08-07 sanasida arxivlangan)
- ↑ „Ionic bond“,IUPAC Compendium of Chemical Terminology, 2009. DOI:10.1351/goldbook.IT07058. ISBN 978-0-9678550-9-7.
- ↑ David Arthur Johnson, Metals and Chemical Change, Open University, Royal Society of Chemistry, 2002, ISBN 0-85404-665-8
- ↑ L. Pauling The Nature of the Chemical Bond (3rd ed., Oxford University Press 1960) p.98-100.
